Согласно современной классификации, цирковирусы выделены в семейство Circoviridae, которое состоит из двух родов – Circovirus и Gyrovirus. В состав рода Circovirus входят ЦВС-1, ЦВС-2 и девять цирковирусов птиц. Недавно цирковирусы были выявлены у лисиц с менингоэнцефалитом, собак с васкулитом, норок с диареей, летучих мышей, в фекалиях человека и обезьян. В культурах клеток размножаются только ЦВС-1, ЦВС-2 и вирус анемии цыплят [6].
Впервые цирковирус свиней обнаружен немецкими исследователями в 1974 году как нецитопатогенный контаминант перевиваемой культуры клеток почек поросят (РК-15). Он оказался непатогенным для свиней [1, 9]. В 1998 году из тканей поросят с синдромом послеотъемного мультисистемного истощения (СПМИ) в культуре клеток РК-15 изолированы новые антигенно родственные между собой штаммы ЦВС, которые отличались от вируса-контаминанта. Цирковирус, установленный как нецитопатогенный контаминант культуры клеток РК-15, обозначили ЦВС-1, а ЦВС, вызывающий у поросят СПМИ, – ЦВС-2 [6, 9].
Все выделенные в различных странах мира штаммы ЦВС-2 имеют близкое антигенное и генетическое родство. Идентичность нуклеотидной последовательности составляет более 93%. На основании генетических различий штаммы ЦВС-2 подразделяют на четыре основных генотипа – ЦВС-2а, ЦВС-2b, ЦВС-2с, ЦВС-2d. Наибольшей патогенностью обладают широко распространенные в свиноводческих хозяйствах многих стран ЦВС-2b и ЦВС-2d [9, 11].
ЦВС-2 обнаруживают при различных заболеваниях, включая СПМИ, синдром дерматита и нефропатии (СДНС), репродуктивные нарушения и респираторные болезни свиней. В Европе их называют цирковирусными болезнями свиней (ЦВБС), а в Северной Америке – цирковирус-ассоциированными болезнями свиней (ЦВАБС) [1, 5, 9]. До применения вакцин ЦВБС причиняли значительный экономический ущерб. Так, в странах ЕС ежегодные потери оценивались в 900 млн евро, в США – $750 млн. Специфическую профилактику этих заболеваний осуществляют с 2006 года с помощью инактивированных и рекомбинантных вакцин, изготовленных из ЦВС-2а или капсидного белка вируса, продуцируемого в бакуловирусной системе. Начиная с двухнедельного возраста поросят иммунизируют вакцинами. В последнее время предлагают иммунизировать не только поросят, но также свиноматок и хряков. Вакцинация хряков сопровождается уменьшением уровня виремии и титра ЦВС-2 в сперме, что приводит к снижению распространения вируса среди репродуктивного поголовья. Вакцинация свиноматок лишь частично предотвращает трансплацентарную передачу вируса плодам и уменьшает количество ЦВС-2 в молозиве и молоке [3, 9].
Коммерческие вакцины против ЦВБС, включая и отечественную «ВЕРРЕС-ЦИРКО», значительно снижают заболеваемость и гибель поросят в период доращивания и откорма, минимизируя возможный экономический ущерб [1, 2, 9].
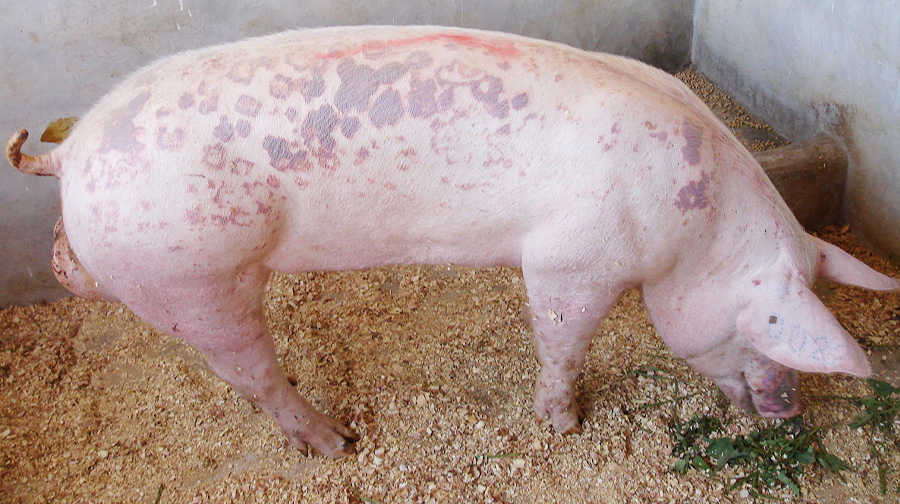
В 2015 году в свиноводческих хозяйствах США наблюдали повышенную смертность свиноматок с клиническими признаками дерматита и нефропатии (СДНС) и нарушениями репродукции (аборты). В диагностических пробах (ткани абортированных плодов и погибших свиноматок) методом количественной полимеразной цепной реакции (ПЦР) не обнаружены ЦВС-2, парвовирус и вирус репродуктивного и респираторного синдрома свиней. С помощью метагеномного анализа в исследованных пробах выявлен новый цирковирус, который обозначен как цирковирус свиней 3-го типа (ЦВС-3). Метагеномный анализ основан на секвенировании всей ДНК и РНК, содержащейся в пробе, и обработке данных биоинформационными методами. Между генами капсидного белка и репликазы ЦВС-3 и ЦВС-2 имеется только 37% гомологии [7].
С помощью разработанной количественной ПЦР в тканевых гомогенатах мертвых плодов обнаружен высокий уровень геномных копий ЦВС-3 (7,6х107 в 1 мл). В тканях свиноматок с поражениями кожи их содержание было на несколько порядков ниже. При исследовании фиксированных формалином проб тканей от 48 свиноматок, погибших с признаками СДНС в течение 2010–2016 годов, ДНК ЦВС-3 обнаружена у 45 животных (93,8%). Все пробы для ретроспективного исследования не содержали ЦВС-2.
Специфические антитела в сыворотке крови свиней определяли методом ИФА с использованием в качестве антигена рекомбинантного капсидного белка ЦВС-3. При исследовании 83 проб сывороток крови в 46 (55%) выявлены антитела к ЦВС-3. Положительные пробы получены от свиней из шести штатов США [7]. Попытки размножения вируса в перевиваемых культурах клеток ST и PK-15 закончились безрезультатно. Клетки были инокулированы гомогенатами тканей плодов, содержащих ЦВС-3 и пассированных три раза.
В 2016 году в свиноводческих хозяйствах Китая наблюдалась повышенная смертность свиноматок (5,4–10,5%) с нарушением репродукции: рождение мертвых поросят составляло от 5,2% до 20,1%. Методом ПЦР было исключено инфицирование свиней вирусами классической чумы, болезни Ауески, ЦВС-2, репродуктивного и респираторного синдрома, эпизоотической диареи, трансмиссивного гастроэнтерита и ротавирусной болезни свиней. В исследованных пробах обнаружили новый цирковирус свиней – ЦВС-3. Для выяснения его распространения в свиноводческих хозяйствах Китая были исследованы 222 диагностические пробы (ткани мертвых поросят и свиноматок, сыворотка крови, сперма) из 35 хозяйств 11 провинций. ЦВС-3 обнаружили в пробах 24 хозяйств (68,6%) из 35. Из 222 изученных проб 77 (34,7%) оказались положительными. ЦВС-3 находили в мозге, легких, лимфоузлах, миндалинах, сперме и сыворотке крови. В 35 пробах (15,8%) были выявлены два цирковируса – ЦВС-3 и ЦВС-2 [4].
Полная нуклеотидная последовательность генома определена у девяти изолятов ЦВС-3 и частичная (гена капсидного белка) – у 33 изолятов. Идентичность нуклеотидной последовательности генома китайских и американских изолятов составляла 99,0–99,1%, а гена капсидного белка – 98,4–98,9%. Китайские изоляты ЦВС-3 подразделены на два подтипа – ЦВС-3а и ЦВС-3b. Американские изоляты относятся к подтипу ЦВС-3а [4]. Кроме того, в свиноводческих хозяйствах США и Китая также был обнаружен ЦВС-3 у поросят с пневмонией, лихорадкой, анорексией и поражением суставов в период доращивания [8, 10].
В «Научно-исследовательском институте диагностики и профилактики болезней человека и животных» разработаны методы определения нового цирковируса свиней (ЦВС-3) в диагностических пробах и проводят исследования по выяснению распространения этого вируса в свиноводческих хозяйствах нашей страны.
Литература
- Орлянкин Б. Г. Цирковирусные болезни свиней: Распространение, диагностика и специфическая профилактика. Ветеринария, 2013. №8. С. 3–9.
- Орлянкин Б. Г., Мишин А. М., Котельников А. П., Алипер Т. И. Эффективность отечественной рекомбинантной вакцины «ВЕРРЕС-ЦИРКО» в свиноводстве. Ветеринария, 2014. №5. С.9–11.
- Beach N. M., Meng X. J. Efficacy and future prospects of commercially available and experimental vaccines against porcine Circovirus type 2 (PCV2).Virus Res., 2012. V. 164. P. 33–
- Ku X., Chen F., Li P. et al. Identification and genetic characterization of porcine Circovirus type 3 in China. Transbound. Emerg. Dis., 2016.
- Madson D. M., Opriessnig T. Effect of porcine Circovirus type 2 (PCV2) infection on reproduction: Disease, vertical transmission, diagnostics and vaccination. Anim. Health Res. Rev., 2011. 12. P. 47–65.
- Meng X. J. Circoviridae. Fields virology. 6th Philadelphia, 2013. V. 2. P. 1792–1801.
- Palinski R., Pineyro P., Shang P. et al. A novel porcine Circovirus distantly related to know Circoviruses with porcine Dermatitis and Nephropathy syndrome and Reproductive failure. J., 2016.
- Phan T. G., Gianniti F., Rossow S. et al. Detection of a novel Circovirus PCV3 in pigs with cardiac and multi-systemic inflammation. Virol. J., 2016.
- Segales J., Allan G. M., Domingo M. Porcine Circoviruses. Diseases of swine. 10th Wiley-Blackwell, 2012. P. 405–417.
- Shen H., Liu X., Zhang P. et al. Genomic characterization a porcine Circovirus type 3 in South China. Transbound. Emerg. Dis., 2017.
- Xiao C. T., Halbur P. G., Opriessnig T. Global molecular genetic analysis of porcine Circovirus type 2 (PCV2) sequence confirms the presence of four main PCV2 genotypes and reveals a rapid increase of PCV2d. J. Gen. Virol., 2015. 96. P. 1830–1841.